Давно известно, что все молекулы обладают двумя равными и противоположными зарядами, которые разделены определенным расстоянием. В случае таких полярных молекул центр отрицательного заряда не совпадает с центром положительного заряда. Степень полярности в таких ковалентных молекулах может быть описана термином дипольный момент, который по существу является мерой полярности в полярной ковалентной связи.
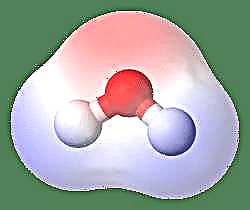
Простейшим примером диполя является молекула воды. Молекула воды является полярной из-за неравного распределения ее электронов в «изогнутой» структуре. Молекула воды образует угол с атомами водорода на концах и кислородом в вершине. Поскольку кислород имеет более высокую электроотрицательность, чем водород, сторона молекулы с атомом кислорода имеет частичный отрицательный заряд, в то время как водород в центре имеет частичный положительный заряд. Из-за этого направление дипольного момента указывает на кислород.
На физическом языке электрический дипольный момент является мерой разделения положительных и отрицательных электрических зарядов в системе зарядов, то есть мерой общей полярности системы заряда, то есть разделения электрического заряда молекул, которое приводит к диполю. Математически, и в простом случае двух точечных зарядов, одного с зарядом + q и одного с зарядом? Q, электрический дипольный момент p может быть выражен как: p = qd, где d - вектор смещения, указывающий от отрицательного заряда на положительный заряд. Таким образом, вектор электрического дипольного момента p направлен от отрицательного заряда к положительному заряду.
Еще один способ взглянуть на это - представить дипольный момент греческой буквой m, m = ed, где e - электрический заряд, а d - расстояние разделения. Он выражается в единицах Дебая и записывается как D (где 1 Дебай = 1 x 10-18e.s.u см). Дипольный момент является векторной величиной и поэтому представлен маленькой стрелкой с хвостом в положительном центре и головой, указывающей на отрицательный центр. В случае молекулы воды дипольный момент равен 1,85 D, тогда как молекула соляной кислоты равна 1,03 D и может быть представлена как:
Мы написали много статей о дипольном моменте для журнала Space. Вот статья о том, из чего состоит вода, и статья о молекулах.
Если вам нужна дополнительная информация о дипольном моменте, ознакомьтесь с этими статьями из Hyperphysics and Science Daily.
Мы также записали целый эпизод «Астрономического актера», посвященный молекулам в космосе. Послушайте, Эпизод 116: Молекулы в Космосе.
Источники:
http://en.wikipedia.org/wiki/Electric_dipole_moment
http://en.wikipedia.org/wiki/Dipole
http://www.tutorvista.com/content/chemistry/chemistry-iii/chemical-bonding/degree-polarity.php
http://hyperphysics.phy-astr.gsu.edu/hbase/electric/dipole.html#c1
http://en.wikipedia.org/wiki/Water_molecule